Reazione di Eschweiler-Clarke
La Reazione di Eschweiler–Clarke (conosciuta anche come Metilazione di Eschweiler–Clarke) è una reazione chimica attraverso la quale un'ammina primaria (o secondaria) viene metilata usando un eccesso di acido formico e formaldeide.[1][2][3][4] Reazioni di amminazioni riduttive come questa non producono sali d'ammonio quaternari, ma si fermano allo stadio di ammina terziaria. Questa reazione prende il nome dal chimico tedesco Wilhelm Eschweiler (1860–1936) e dal collega inglese Hans Thacher Clarke (1887-1972).

Meccanismo[modifica | modifica wikitesto]
La prima metilazione dell'ammina inizia con la formazione dell'immina per opera della formaldeide. L'acido formico agisce da fonte di ione idruro e riduce l'immina in ammina secondaria. La driving force della reazione è la formazione di diossido di carbonio gassoso. La formazione dell'ammina terziaria avviene in maniera simile ma più lentamente a causa della difficoltà dovuta alla formazione dello ione imminio.
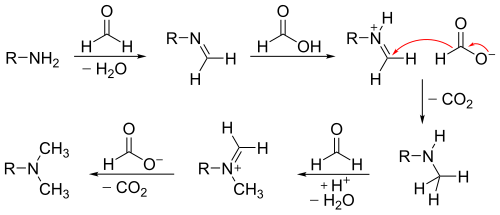
Dal meccanismo si può facilmente comprendere che il sale d'ammonio quaternario non si forma, in quanto è impossibile per un'ammina terziaria formare un'altra immina o ione imminio.
Solitamente le ammine chirali non racemizzano sotto queste condizioni di reazione.[5]
Una versione alternativa di questa reazione sostituisce l'acido formico con sodio cianoboroidruro.
Note[modifica | modifica wikitesto]
- ^ Eschweiler, W., Ersatz von an Stickstoff gebundenen Wasserstoffatomen durch die Methylgruppe mit Hülfe von Formaldehyd, in Ber., vol. 38, 1905, p. 880, DOI:10.1002/cber.190503801154.
- ^ H. T. Clarke, H. B. Gillespie e S. Z. Weisshaus, The Action of Formaldehyde on Amines and Amino Acids, in Journal of the American Chemical Society, vol. 55, n. 11, 1933, p. 4571, DOI:10.1021/ja01338a041.
- ^ Moore, M. L., The Leuckart Reaction, in Org. React., vol. 5, 1949, pp. 301-330, DOI:10.1002/0471264180.or005.07.
- ^ Icke, R. N., Wisegarver, B. B. e Alles, G. A., β-Phenylethyldimethylamine, Organic Syntheses, 1945.
- ^ Eugene Farkas e Cheryl J. Sunman, Chiral synthesis of doxpicomine, in J. Org. Chem., vol. 50, n. 7, 1985, p. 1110, DOI:10.1021/jo00207a037.)
Voci correlate[modifica | modifica wikitesto]
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su Reazione di Eschweiler-Clarke
Wikimedia Commons contiene immagini o altri file su Reazione di Eschweiler-Clarke