2-eptanone
| 2-eptanone | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| eptan-2-one | |
| Nomi alternativi | |
| amil metil chetone butilacetone metil n-amil chetone metil pentil chetone | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C7H14O |
| Massa molecolare (u) | 114,18 |
| Aspetto | liquido incolore |
| Numero CAS | |
| Numero EINECS | 203-767-1 |
| PubChem | 8051 |
| SMILES | CCCCCC(=O)C |
| Proprietà chimico-fisiche | |
| Densità (g/l, in c.s.) | 0,8 |
| Temperatura di fusione | −35.5 °C (237,65 K) |
| Temperatura di ebollizione | 151 °C (424,15 K) |
| Tensione di vapore (Pa) a 298,15 K | 20 |
| Indicazioni di sicurezza | |
| Punto di fiamma | 39 °C (312,15 K) |
| Limiti di esplosione | 1% - 5,5% |
| Temperatura di autoignizione | 393 °C (666,15 K) |
| Simboli di rischio chimico | |
 
| |
| attenzione | |
| Frasi H | 226 - 302 - 332 |
| Consigli P | --- [1] |
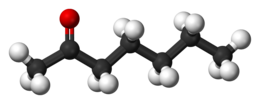
Il 2-eptanone è un chetone. Ha formula bruta C7H14O; presenta una catena di 7 atomi di carbonio, il secondo dei quali è legato, mediante un doppio legame, ad un atomo di ossigeno. È un liquido incolore, simile all'acqua, con un odore fruttato simile a quello di banana.[2]
Il 2-eptanone viene secreto dalle ghiandole mandibolari delle api operaie come feromone d'allarme.
Il 2-eptanone è elencato dalla FDA come "additivo alimentare autorizzato per aggiunta diretta al cibo destinato al consumo umano" (21 CFR 172.515) e si presenta naturalmente in alcuni alimenti (ad es. birra, pane bianco, burro, formaggi vari e patate patatine fritte).[3]
È stato studiato il meccanismo d'azione del 2-eptanone come feromone nei recettori degli odori nei roditori.[4][5][6] Il 2-eptanone è presente nelle urine di ratti stressati e crede che sia usato come mezzo per allertare altri ratti.[6][7] Alcune specie di vermi sono attratte dal 2-eptanone e i batteri possono usarlo come mezzo di partenogenesi.[8] È stato anche scoperto che il 2-eptanone viene escreto dalle api da miele quando mordono piccoli parassiti all'interno della colonia come larve di falene e Varroa destructor. Sebbene si credesse storicamente un feromone di allarme, il 2-eptanone ha dimostrato di agire come anestetico sui parassiti, consentendo all'ape di miele di stordire il parassita ed espellerlo dall'alveare. Questo studio potrebbe portare all'uso del 2-eptanone come anestetico locale alternativo alla lidocaina, che sebbene ben consolidato per l'uso clinico, ha lo svantaggio di provocare reazioni allergiche in alcune persone.[9]
Il 2-eptanone era uno dei metaboliti dell'n-eptano trovato nelle urine dei dipendenti esposti all'eptano nelle fabbriche di scarpe e pneumatici.[10] Ciò si verifica comunemente dall'esposizione ai plastificanti.[11] Il 2-eptanone può essere assorbito attraverso la pelle, inalato e consumato.[12] L'esposizione al 2-eptanone può causare irritazione a pelle/occhi, apparato respiratorio, mal di testa, vomito e nausea.[12]
Note[modifica | modifica wikitesto]
- ^ Sigma Aldrich; rev. del 01.03.2013
- ^ 2-Heptanone, in PubChem, National Center for Biotechnology Information, U.S. National Library of Medicine. URL consultato il 7 marzo 2019.
- ^ Methyl (n-amyl) ketone, Chemical Sampling Information, Occupational Safety & Health Administration
- ^ Wang Z, Balet Sindreu C, Li V, Nudelman A, Chan GC, Storm DR, Pheromone detection in male mice depends on signaling through the type 3 adenylyl cyclase in the main olfactory epithelium, in The Journal of Neuroscience, vol. 26, n. 28, July 2006, pp. 7375–9, DOI:10.1523/JNEUROSCI.1967-06.2006, PMID 16837584.
- ^ Hauser R, Marczak M, Karaszewski B, Wiergowski M, Kaliszan M, Penkowski M, Kernbach-Wighton G, Jankowski Z, Namieśnik J, A preliminary study for identifying olfactory markers of fear in the rat, in Lab Animal, vol. 37, n. 2, February 2008, pp. 76–80, DOI:10.1038/laban0208-76, PMID 18216798.
- ^ a b Gutiérrez-García AG, Contreras CM, Mendoza-López MR, García-Barradas O, Cruz-Sánchez JS, Urine from stressed rats increases immobility in receptor rats forced to swim: role of 2-heptanone, in Physiology & Behavior, vol. 91, n. 1, May 2007, pp. 166–72, DOI:10.1016/j.physbeh.2007.02.006, PMID 17408705.
- ^ Gutiérrez-García AG, Contreras CM, Saldivar-Lara M, An alarm pheromone reduces ventral tegmental area-nucleus accumbens shell responsivity, in Neuroscience Letters, vol. 678, June 2018, pp. 16–21, DOI:10.1016/j.neulet.2018.04.054, PMID 29727729.
- ^ Zhang C, Zhao N, Chen Y, Zhang D, Yan J, Zou W, Zhang K, Huang X, The Signaling Pathway of Caenorhabditis elegans Mediates Chemotaxis Response to the Attractant 2-Heptanone in a Trojan Horse-like Pathogenesis, in The Journal of Biological Chemistry, vol. 291, n. 45, November 2016, pp. 23618–23627, DOI:10.1074/jbc.M116.741132, PMC 5095415, PMID 27660389.
- ^ Honey-bees found to have bite that stuns, BBC News, 26 ottobre 2012. URL consultato l'8 gennaio 2013.
- ^ Perbellini L, Brugnone F, Cocheo V, De Rosa E, Bartolucci GB, Identification of the n-heptane metabolites in rat and human urine, in Archives of Toxicology, vol. 58, n. 4, April 1986, pp. 229–34, DOI:10.1007/BF00297111, PMID 3718225.
- ^ Walker V, Mills GA, Urine 4-heptanone: a beta-oxidation product of 2-ethylhexanoic acid from plasticisers, in Clinica Chimica Acta; International Journal of Clinical Chemistry, vol. 306, 1–2, April 2001, pp. 51–61, DOI:10.1016/S0009-8981(01)00390-4, PMID 11282094.
- ^ a b 2-HEPTANONE, in National Library of Medicine HSDB Database. URL consultato il 21 febbraio 2019.
Altri progetti[modifica | modifica wikitesto]
 Wikimedia Commons contiene immagini o altri file su 2-eptanone
Wikimedia Commons contiene immagini o altri file su 2-eptanone
Collegamenti esterni[modifica | modifica wikitesto]
- scheda di sicurezza, su cdc.gov. URL consultato l'11 gennaio 2009 (archiviato dall'url originale il 15 giugno 2008).